技术专题
Nat Biotechnol:证实CRISPR/Cpf1基因组编辑几乎没有脱靶效应
作为CRISPR基因组编辑的新工具,Cpf1因其不同于Cas9的性质而引起人们的广泛关注。它只需要单个RNA,即crRNA(CRISPR RNA),因而组装更加简单;它的交错切割模式可能促进利用所需的序列替换现有的DNA序列;它识别富含胸腺嘧啶的DNA序列,而且相对于Cas9识别的富含鸟嘌呤的序列,人们很少探讨这种序列。总之,Cpf1有望扩大CRISPR基因组编辑靶位点的范围,同时具有更好的编辑效率。
尽管Cpf1有巨大潜力成为一种强大的基因组编辑工具,但是人们很少证实这种新的工具如何特异性地找到它的靶位点。在一项新的研究中,来自韩国基础科学研究所(IBS)基因组编辑中心的研究人员证实作为一种高度特异性的可编程工具,Cpf1适合用于精确的基因组编辑。相关研究结果于2016年6月6日在线发表在Nature Biotechnology期刊上,论文标题为“Genome-wide analysis reveals specificities of Cpf1 endonucleases in human cells”。
研究人员使用了两种类型的Cpf1家族蛋白(AsCpf1和LbCpf),这是因为它们是同类蛋白中编辑效率最高的,并开展Digenome-seq测试:他们设计出的一种测试方法以便在全基因组中鉴定出Cpf1能够进行切割的靶位点(on-target site)和脱靶位点(off-target site)。不含细胞的基因组DNA是从人细胞中分离出的,然后利用事先组装的重组Cpf1核糖核蛋白(RNP,编者注:由crRNA和Cpf1进行组装而形成)对该基因组DNA进行切割,随后进行全基因组测序。通过对对应于体外靶切割位点和脱靶切割位点的测序序列片段进行比对,就可通过计算鉴定出这些位点。
 Figure 1a(左边):在这项研究中,利用单重Digenome-seq确定LbCpf1(n = 8)、AsCpf1(n = 8)和SpCas9(n = 2)的体外切割位点。在我们之前的研究中,利用利用多重Digenome-seq确定SpCas9(n = 11)的体外切割位点。Figure 1b(右边):利用Digenome-seq分析Cpf1和SpCas9 RGENs的全基因组特异性。
Figure 1a(左边):在这项研究中,利用单重Digenome-seq确定LbCpf1(n = 8)、AsCpf1(n = 8)和SpCas9(n = 2)的体外切割位点。在我们之前的研究中,利用利用多重Digenome-seq确定SpCas9(n = 11)的体外切割位点。Figure 1b(右边):利用Digenome-seq分析Cpf1和SpCas9 RGENs的全基因组特异性。
基因组分析表明Cpf1是高度特异性的,与Cas9相比,只有更少的脱靶切割位点(对LbCpf1而言是6个,对AsCpf1而言是12个),而Cas9能够切割人基因组上的90多个位点(Fig. 1a)。特别地,在大多数体外脱靶切割位点中,代表脱靶效应的核苷酸插入或删除(insertion or deletion, indel)发生率低于0.1%,远低于对应的靶位点上的indel发生率,这提示着这两种Cpf1蛋白几乎没有脱靶效应。作为这篇论文的共同第一作者,KIM Daesik说,“值得注意的是,靶向某个位点的LbCpf1和AsCpf1在整个人基因组中只切割靶位点。”
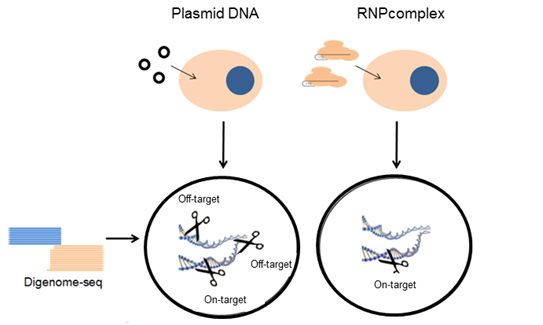
Figure 2:通过运送Cpf1和crRNA形成RNP复合物而不是编码Cpf1和crRNA的质粒,可避免Cpf1脱靶效应。
论文通信作者、IBS基因组编辑中心主任KIM Jin-Soo说,“为了降低脱靶效应,我们将事先组装的Cpf1 RNP导入细胞中,并且假定Cpf1 RNP与Cas9 RNP一样将在转染后立即切割靶位点,并且被破坏蛋白的内源性酶快速地降解,因而在不牺牲靶标切割效率的同时降低脱靶效应。”确实,Cpf1 RNP并不诱导足以在脱靶位点产生突变的高水平indel发生(Fig. 2)。
Jin-Soo认为,鉴于这项研究证明了Cpf1优越的特异性,这种新的核酸内切酶将能够更加广泛地用于精确的基因组编辑,同时不会产生任何不想到的突变。CRISPR/Cpf1的应用将是没有限制的,从无毒性抗癌药物和干细胞治疗等治疗方法到高附加值的牲畜和农产品,而且也一直是开放的。
